M. Of. nr.
901 din 4 octombrie 2004
PARLAMENTUL ROMÂNIEI
CAMERA DEPUTAŢILOR SENATUL
L E G E
pentru
modificarea şi completarea Legii nr. 178/2000 privind produsele cosmetice
Parlamentul României adoptă prezenta lege.
Art. I. – Legea nr. 178/2000
privind produsele cosmetice, publicată în Monitorul Oficial al României, Partea
I, nr. 525 din 25 octombrie 2000, cu modificările şi completările
ulterioare, se modifică şi se completează după cum urmează:
1. La articolul 2,
litera a) va avea următorul cuprins:
„a) produs cosmetic – orice
substanţă sau preparat care urmează să fie pus în contact cu diverse părţi
externe ale corpului uman, precum piele, păr, unghii, buze, organe genitale
externe sau cu dinţii şi mucoasa bucală, cu scopul exclusiv sau principal de a
le curăţa, a le parfuma, a le modifica aspectul şi/sau a le corecta mirosurile
corporale şi/sau a le proteja ori a le menţine în bună stare;“
2. La articolul 2,
după litera k) se introduc trei litere noi, literele l), m) şi n), cu
următorul cuprins:
„l) produs cosmetic
finit – produsul cosmetic în formula sa finală, aşa cum este
introdus pe piaţă şi oferit consumatorului final, sau prototipul acestuia;
m) prototip – primul
model sau design al unui produs cosmetic care nu a fost fabricat în loturi şi
de la care produsul cosmetic finit este copiat sau dezvoltat;
n) perioada după
deschidere – perioada de timp în care un produs cosmetic finit
poate fi folosit în siguranţă, calculată din momentul primei deschideri a
ambalajului primar şi începerii utilizării produsului.“
3. Articolul 3 va
avea următorul cuprins:
„Art. 3. – Lista
cuprinzând categoriile de produse cosmetice, aşa cum sunt definite în cuprinsul
art. 2 lit. a), este prevăzută în anexa nr. 1.“
4. După articolul 3
se introduce un articol nou, articolul 31, cu următorul cuprins:
„Art. 31. – Ministerul Sănătăţii
reprezintă autoritatea naţională competentă pentru reglementarea comercializării
produselor cosmetice, notificarea acestora în întocmirea şi administrarea bazei
de date, inspecţia şi controlul pe piaţă, informarea populaţiei, înregistrarea
cazurilor semnalate privind efectele adverse asupra populaţiei, cauzate de
produsele cosmetice, raportarea către Comisia Europeană.“
5. Articolul 4 va
avea următorul cuprins:
„Art. 4. – Produsele
cosmetice puse pe piaţă nu trebuie să pericliteze sănătatea umană atunci când
sunt folosite în condiţii normale sau raţional previzibile de folosire, ţinându-se
seama, în special, de prezentarea produsului, etichetarea, instrucţiunile privind
utilizarea şi îndepărtarea acestuia, precum şi de orice altă indicaţie prevăzută
de producător, de reprezentantul său autorizat sau de orice altă persoană
responsabilă pentru introducerea pe piaţă a produsului. Aceste indicaţii
nu vor scuti nici o persoană, în nici o circumstanţă, de a se conforma cu alte
dispoziţii ale prezentei legi.“
6. După articolul 5
se introduc articolele 51 şi 52 cu următorul cuprins:
„Art. 51. – (1) Fără
a se prejudicia îndeplinirea obligaţiilor ce derivă din art. 4, se interzice:
a) introducerea pe piaţă
a produselor cosmetice în legătură cu formula finală, cât şi a celor conţinând
ingrediente sau combinaţii de ingrediente care, pentru a îndeplini cerinţele
prezentei legi, au fost testate pe animale, folosindu-se o metodă, alta decât
cea alternativă, după data la care aceasta din urmă a fost validată şi adoptată
la nivelul Uniunii Europene, ţinându-se seama de evoluţia procesului de
validare din cadrul Organizaţiei pentru Cooperare şi Dezvoltare Economică;
b) testarea pe animale
a produselor cosmetice finite, pentru a îndeplini cerinţele prezentei legi;
c) testarea pe animale
a ingredientelor sau combinaţiilor de ingrediente, pentru a îndeplini cerinţele
prezentei legi, începând cu data la care aceste teste trebuie să fie înlocuite
de metodele alternative validate sau stabilite de către Comisia Europeană. Metodele
alternative sunt prevăzute în anexa nr. 3 la Normele metodologice de
aplicare a Ordonanţei de urgenţă a Guvernului nr. 200/2000 privind
clasificarea, etichetarea şi ambalarea substanţelor şi preparatelor chimice
periculoase, aprobate prin Hotărârea Guvernului nr. 490/2002.
(2) Ministerul Sănătăţii
asigură, prin ordin al ministrului, preluarea noilor metode alternative, în
acord cu progresul realizat în validarea şi adoptarea acestora de către Comisia
Europeană, în conformitate cu următoarele termene limită: 11 martie 2009,
pentru testarea ingredientelor sau combinaţiilor de ingrediente, şi 11 martie
2013, pentru testele de toxicitate cu doză repetată, toxicitate reproductivă şi
toxicocinetică.
(3) În situaţii excepţionale,
atunci cînd există un motiv întemeiat în ceea ce priveşte siguranţa unui
ingredient cosmetic existent, Ministerul Sănătăţii poate solicita Comisiei
Europene să acorde o derogare de la prevederile alin. (1). Cererea de
derogare trebuie să conţină o evaluare a situaţiei şi să indice măsurile
necesare. Pe baza cererii şi după consultarea Comitetului Ştiinţific
pentru Cosmetice şi Produse Nealimentare, Comisia Europeană poate autoriza
derogarea prin decizie motivată. Această autorizare trebuie să conţină
condiţiile în care s-a acordat derogarea, obiectivul specific, durata şi
raportarea rezultatelor.
(4) Derogarea poate fi
acordată numai dacă:
a) ingredientul se
foloseşte în mod frecvent şi nu poate fi înlocuit de un alt ingredient cu funcţie
similară;
b) problema de sănătate
umană specifică este fundamentată şi nevoia de a recurge la testări pe animale
este justificată şi susţinută de un protocol de cercetare detaliat, propus ca
bază de evaluare.
Art. 52. – (1) Este
interzisă folosirea în produsele cosmetice a substanţelor clasificate ca fiind
cancerigene, mutagenice sau toxice pentru reproducere, din categoriile 1, 2 şi
3, aşa cum sunt prevăzute în anexa nr. 2 la Normele metodologice de
aplicare a Ordonanţei de urgenţă a Guvernului nr. 200/2000 privind
clasificarea, etichetarea şi ambalarea substanţelor şi preparatelor chimice
periculoase.
(2) O substanţă
clasificată în categoria 3 poate fi folosită în produsele cosmetice numai dacă
a fost evaluată de Comitetul Ştiinţific pentru Cosmetice şi Produse
Nealimentare al Comisiei Europene şi a fost acceptată pentru a fi folosită în
produse cosmetice.“
7. După articolul 6
se introduce articolul 61 cu următorul cuprins:
„Art. 61. – (1) Prin
derogare de la prevederile art. 5 şi fără a aduce atingere prevederilor
Ordinului ministrului industriei şi resurselor şi al ministrului sănătăţii şi
familiei nr. 309/729/2001 privind inventarul pentru ingredientele folosite
în produsele cosmetice, publicat în Monitorul Oficial al României, Partea I, nr. 756
din 28 noiembrie 2001, Ministerul Sănătăţii poate autoriza folosirea pe
teritoriul României a substanţelor care nu sunt prevăzute în lista de substanţe
permise pentru anumite produse cosmetice, în următoarele condiţii:
a) autorizarea trebuie
să se limiteze la o perioadă maximă de 3 ani;
b) să se efectueze o
verificare oficială a produselor cosmetice care conţin substanţa sau preparatul
a cărui utilizare a fost autorizată;
c) produsul cosmetic
astfel fabricat trebuie să poarte o indicaţie distinctă, care va fi precizată în
autorizaţie.
(2) Ministerul Sănătăţii
trebuie să informeze Comisia Europeană şi statele membre despre decizia de
autorizare luată conform alin. (1), în decurs de două luni de la data intrării
în vigoare a autorizaţiei.
(3) Înainte de
expirarea termenului de 3 ani, prevăzut la alin. (1) lit. a),
Ministerul Sănătăţii poate înainta Comisiei Europene o cerere pentru includerea
pe lista substanţelor permise a substanţei care a primit autorizarea naţională,
conform alin. (1). Concomitent va comunica documentaţia pe care se întemeiază
această cerere şi va indica utilizările cărora le este destinată substanţa.“
8. La articolul 8,
partea introductivă va avea următorul cuprins:
„Art. 8. – Notificarea
constă în transmiterea, în formă scrisă şi/sau electronică, a următoarelor
date:“
9. Alineatele (1) şi
(3) ale articolului 9 vor avea următorul cuprins:
„Art. 9. – (1) Notificarea
unui produs cosmetic care se introduce pe piaţă pe teritoriul României se face la
Ministerul Sănătăţii, prin transmiterea în formă scrisă şi/sau electronică a
formularului de notificare. Ministerul Sănătăţii înregistrează
notificarea, comunică celui care a transmis-o numărul notificării şi face
publică lista produselor cosmetice notificate.
….......................................................................................
(3) Orice modificare a
informaţiilor transmise Ministerului Sănătăţii, conform prevederilor art. 8,
va fi adusă la cunoştinţă acestuia în termen de 30 de zile de la data apariţiei
modificării.“
10. La articolul 10
alineatul (1), literele b), d), e) şi f) vor avea următorul cuprins:
„b) specificaţiile
fizico-chimice şi microbiologice pentru materiile prime şi produsul finit şi
criteriile de control de puritate şi microbiologie pentru produsul cosmetic;
........................................................................................…
d) numele persoanei
responsabile cu fabricarea sau importul pentru prima dată al unui produs
cosmetic în Uniunea Europeană; persoana responsabilă trebuie să posede un nivel
adecvat de calificare profesională sau experienţă, în conformitate cu legislaţia
şi practica statului membru al Uniunii Europene unde sunt fabricate sau unde
sunt prima dată importate produsele cosmetice;
e) evaluarea riscului
pentru sănătatea umană al produsului cosmetic. Pentru aceasta fabricantul
va ţine seama de profilul toxicologic general al ingredientelor folosite, de
structura lor chimică şi de nivelul de expunere, în special de caracteristicile
de expunere specifice zonei în care produsul va fi aplicat sau de populaţia căreia
îi este destinat; pentru produsele destinate copiilor sub 3 ani, precum şi
pentru cele destinate exclusiv igienei intime externe trebuie să existe o
evaluare specifică a securităţii pentru sănătatea umană. În cazul în care
produsul se fabrică în diferite localităţi pe teritoriul României sau al
statelor membre ale Uniunii Europene, producătorul poate să aleagă o singură
locaţie/loc, unde informaţiile privind produsul sunt disponibile. În acest
sens, la solicitarea autorităţilor competente pentru monitorizarea produsului
sau a altor autorităţi cu competenţe de control, producătorul este obligat să
precizeze adresa la care informaţiile sunt rapid accesibile;
f) numele şi adresa
persoanelor calificate responsabile, care au evaluat produsul din punctul de
vedere al siguranţei pentru sănătatea umană; persoanele responsabile pentru
evaluare trebuie să aibă diplomă de studii superioare în specialităţile:
farmacie, toxicologie, dermatologie, medicină sau o specialitate similară, aşa
cum este definită în cuprinsul Legii nr. 200/2004 privind recunoaşterea
diplomelor şi calificărilor profesionale pentru profesiile reglementate din România.“
11. La articolul 10
alineatul (1), după litera h) se introduce litera i) cu următorul
cuprins:
„i) informaţii privind
orice testări pe animale, efectuate de producător, agenţii sau furnizorii săi,
legate de dezvoltarea produsului sau de evaluarea siguranţei produsului
cosmetic ori a ingredientelor sale, inclusiv orice testare pe animale, efectuată
în scopul respectării unor reglementări naţionale din ţările care nu sunt
membre ale Uniunii Europene.“
12. La articolul 10,
după alineatul (2) se introduc alineatele (3) şi (4) cu următorul
cuprins:
„(3) Fără a se aduce
prejudicii protejării secretului comercial şi proprietăţii intelectuale, producătorul,
reprezentantul său autorizat, beneficiarul fabricării produsului cosmetic sau
persoana responsabilă cu introducerea pe piaţă a unui produs cosmetic importat
va asigura ca informaţia prevăzută la alin. (1) lit. a) şi
g) să fie accesibilă publicului în orice format, inclusiv electronic;
informaţiile prevăzute la alin. (1) lit. a), care vor fi
accesibile publicului, vor fi limitate la informaţiile cantitative ale substanţelor
periculoase reglementate prin Ordonanţa de urgenţă a Guvernului nr. 200/2000
privind clasificarea, etichetarea şi ambalarea substanţelor şi preparatelor
chimice periculoase, aprobată cu modificări şi completări prin Legea nr. 451/2001.
(4) Evaluarea siguranţei
pentru sănătatea umană, aşa cum este prevăzută la art. 10 alin. (1) lit. e),
va fi efectuată în conformitate cu principiile de bună practică de laborator
prevăzute de Hotărârea Guvernului nr. 63/2002 privind aprobarea
Principiilor de bună practică de laborator, precum şi inspecţia şi verificarea
respectării acestora în cazul testărilor efectuate asupra substanţelor
chimice.“
13. La articolul 13,
partea introductivă a alineatului (1), literele a), b), c), e), f) şi i) şi
alineatul (2) vor avea următorul cuprins:
„Art. 13. – (1) Produsele
cosmetice pot fi puse pe piaţă numai dacă pe recipient şi pe ambalaj informaţiile
următoare sunt inscripţionate vizibil, lizibil şi cu caractere care nu se şterg
uşor; în ceea ce priveşte informaţiile prevăzute la lit. i), acestea pot
fi inscripţionate doar pe ambalaj. Se vor indica următoarele date:
a) numele sau denumirea
producătorului ori a persoanei responsabile cu introducerea pe piaţă stabilite în
Uniunea Europeană sau abrevierea, dacă aceasta permite identificarea
persoanelor respective;
b) sediul sau adresa
din statul membru al Uniunii Europene a producătorului sau a persoanei
responsabile pentru introducerea pe piaţă în Uniunea Europeană a unui produs
cosmetic importat sau abrevierea sa, atât timp cât aceasta este posibil de
identificat;
c) ţara de origine pentru produsele fabricate în afara statelor membre ale Uniunii Europene;
…........................................................................................
e) data de minimă durabilitate
indicată prin sintagma «A se folosi preferabil înainte de...», urmată de dată
sau de indicarea locului de pe ambalaj unde se află inscripţionată această dată. Data
trebuie clar menţionată, indicându-se, în ordine şi cu cifre arabe, fie luna şi
anul, fie ziua, luna şi anul. Dacă este necesar, această informaţie va fi
suplimentată de o indicare a condiţiilor care trebuie îndeplinite pentru a se
garanta durabilitatea afirmată. Indicarea datei de durabilitate nu este
obligatorie pentru produsele cosmetice a căror durabilitate minimă depăşeşte 30
de luni. Pentru acestea menţiunile se completează cu indicarea perioadei,
după deschiderea produsului cosmetic, în care poate fi folosit în siguranţă de
către consumatori. Această informaţie va fi redată prin simbolul prevăzut în
anexa nr. 2, urmat de perioada de utilizare exprimată în luni şi/sau ani;
f) precauţiunile
speciale la utilizare, în special cele referitoare la ingredientele menţionate în
listele prevăzute la art. 6 alin. (1) şi aprobate prin ordin al
ministrului sănătăţii şi care trebuie inscripţionate pe ambalaj, precum şi
informaţiile speciale de avertizare pentru produsele cosmetice de uz
profesional, în special cele pentru coafură. În situaţia în care acest
lucru nu este posibil din motive practice, va fi alăturat un prospect, o
banderolă ori un cartonaş care va conţine informaţiile necesare consumatorilor,
fie abreviat, fie prin utilizarea simbolului prevăzut în anexa nr. 3, care
trebuie să figureze pe recipient şi pe ambalaj;
…........................................................................................
i) lista cuprinzând
ingredientele care fac parte din compoziţia produsului cosmetic, în ordinea
descrescătoare a greutăţii în momentul încorporării lor; această listă este
precedată de cuvântul „ingrediente“. În cazul în care, din motive
practice legate de spaţiu, acest lucru nu este posibil, va fi alăturat un
prospect, o banderolă ori un cartonaş ce trebuie să conţină informaţia necesară
consumatorului şi va fi inscripţionată pe recipient ori pe ambalaj informaţia
abreviată ori simbolul prevăzut prin ordin al ministrului sănătăţii. Se
vor menţiona ingredientele în concentraţie mai mică de 1%, fără o ordine anume,
după cele a căror concentraţie este mai mare de 1%. Coloranţii se pot menţiona
după celelalte ingrediente. Pentru produsele cosmetice decorative
comercializate în mai multe culori/nuanţe se menţionează toţi agenţii de
colorare folosiţi, precedaţi de sintagma „poate conţine“ sau de simbolul
„+/-“. Compoziţiile de parfumare sau de aromatizare şi materiile lor prime
vor fi menţionate prin cuvântul „parfum“, respectiv „aromă“. Substanţele
cuprinse în listele prezentate la art. 6 alin. (1) lit. a) şi
aprobate prin ordin al ministrului sănătăţii, pentru care există menţiunea de a
fi inscripţionate pe ambalaj, vor fi incluse pe lista ingredientelor,
indiferent de funcţiunea pe care o au în produsul cosmetic.
(2) Acolo unde, din
motive practice legate de dimensiunea sau de forma recipientelor ori a
ambalajelor, nu este realizabilă inscripţionarea informaţiilor prevăzute la
alin. (1) lit. f) şi i), acestea se înscriu pe o etichetă,
o banderolă, un prospect sau un pliant care este alăturat produsului. În
cazul săpunului, al bilelor pentru baie sau al altor produse de dimensiuni
mici, unde este practic imposibil, din motive de dimensiune sau formă, să fie
scrise informaţiile prevăzute la alin. (1) lit. i) pe un
prospect, o etichetă, o banderolă, un pliant sau un cartonaş ataşat, aceste
informaţii vor fi scrise pe un pliant pus în imediata vecinătate a
recipientului în care produsul cosmetic este expus spre vânzare.“
14. La articolul 13,
după alineatul (2) se introduce alineatul (3) cu următorul cuprins:
„(3) Pentru produsele
cosmetice care nu sunt preambalate şi care sunt ambalate la punctul de vânzare
la cererea cumpărătorului ori care sunt preambalate pentru imediata vânzare,
regulile detaliate pentru modul de indicare a informaţiilor prevăzute la alin. (1) se
aprobă prin ordin al ministrului sănătăţii, care se publică în Monitorul
Oficial al României, Partea I.“
15. După articolul
14 se introduce articolul 141 cu următorul cuprins:
„Art. 141. – (1) Ministerul
Sănătăţii nu poate interzice, restrânge sau împiedica introducerea pe piaţă a
produselor cosmetice care îndeplinesc cerinţele prevăzute de prezenta lege.
(2) În vederea asigurării
unui tratament medical prompt şi adecvat în cazul unor situaţii cu risc pentru
sănătate, la solicitarea Ministerului Sănătăţii, producătorul, importatorul sau
persoana responsabilă cu introducerea pe piaţă trebuie să asigure furnizarea
informaţiilor necesare şi adecvate privind substanţele folosite în produsele
cosmetice.
(3) Ministerul Sănătăţii
este autoritatea naţională competentă care asigură transmiterea informaţiilor
prevăzute la alin. (2) către oricare dintre statele membre ale
Uniunii Europene, la solicitarea acestora, luând măsurile necesare pentru ca
informaţia să fie transmisă doar în scopul aplicării unui tratament medical
adecvat.“
16. Articolul 15 va
avea următorul cuprins:
„Art. 15. – (1) În
etichetare, prezentarea spre vânzare sau promovarea produsului se interzice întrebuinţarea
textelor, denumirilor, mărcilor, imaginilor sau a altor însemne care atribuie
produselor caracteristici pe care acestea nu le au.
(2) Producătorul ori
persoana responsabilă cu introducerea pe piaţă a produsului poate menţiona, pe
ambalaj sau pe orice alt document, nota, eticheta, banderola ce însoţeşte ori
care se referă la produs, că produsul nu a fost testat pe animale, numai dacă
producătorul sau furnizorul său de materii prime nu a efectuat testări pe
animale pentru produsul final ori pentru prototip sau nu a folosit nici un
ingredient testat pe animale de către terţe persoane, în scopul formulării de
produse cosmetice noi.“
17. La articolul 17,
partea introductivă şi litera c) vor avea următorul cuprins:
„Art. 17. – Constituie
contravenţii şi se sancţionează cu amendă următoarele fapte:
............................................................................................
c) nerespectarea
prevederilor art. 4, 5, 51, 52, 7, art. 141 alin. (2) şi ale
art. 19, cu amendă de la 50.000.000 lei la 100.000.000 lei.“
18. Articolul 19 va
avea următorul cuprins:
„Art. 19. – În
cazul în care Ministerul Sănătăţii constată, pe baza unor dovezi întemeiate, că
un produs cosmetic, deşi respectă cerinţele prezentei legi, reprezintă un
pericol pentru sănătate, poate interzice provizoriu comercializarea acelui
produs sau poate impune condiţii speciale pentru comercializarea acestuia pe
teritoriul României. În acest caz va informa imediat Comisia Europeană şi
statele membre ale Uniunii Europene asupra acestei decizii şi asupra motivelor
care au fundamentat această decizie.“
19. După articolul
20 se introduc articolele 201 şi 202 cu următorul cuprins:
„Art. 201. – (1) Ministerul
Sănătăţii este autoritatea naţională competentă, care transmite informaţii
Comisiei Europene referitoare la dispoziţiile art. 8 şi 10, în scopul
publicării în Jurnalul Oficial al Comunităţilor Europene.
(2) Ministerul Sănătăţii
asigură cooperarea cu autorităţile competente ale statelor membre, pentru
aplicarea dispoziţiilor prezentei legi.
Art. 202. – În cazul în
care Ministerul Sănătăţii a decis, potrivit art. 19, interzicerea
provizorie sau restricţionarea comercializării unui produs cosmetic, acesta
informează în scris, în termen de 72 de ore, partea interesată/implicată despre
această măsură, indicând motivele deciziei şi măsurile de remediere
recomandate, în conformitate cu reglementările legale existente, precum şi data
limită până la care acestea pot fi aplicate.“
20. Articolul 21 va
avea următorul cuprins:
„Art. 21. – Prevederile
art. 17 se completează cu dispoziţiile Ordonanţei Guvernului nr. 2/2001
privind regimul juridic al contravenţiilor, aprobată cu modificări şi completări
prin Legea nr. 180/2002, cu modificările ulterioare.“
21. După articolul
22 se introduc articolele 221 şi 222 cu următorul cuprins:
„Art. 221. – Ministerul Sănătăţii
va stabili, până la data de 31 decembrie 2006, procedura prin care unele
substanţe şi preparate chimice pot fi autorizate temporar, pentru a fi
utilizate în produsele cosmetice, mecanismul de acces la informaţiile despre
substanţele folosite în fabricarea produselor cosmetice necesare pentru
asigurarea tratamentelor medicale adecvate în cazul unor situaţii cu risc
pentru sănătate, care se aprobă prin ordin al ministrului sănătăţii.
Art. 222. – Prevederile
prezentei legi nu se aplică produselor care conţin substanţe prevăzute în anexa
nr. 6 la Ordinul ministrului sănătăţii şi familiei nr. 1.031/2002
pentru aprobarea listelor cuprinzând substanţele ce pot fi utilizate în compoziţia
produselor cosmetice, publicat în Monitorul Oficial al României, Partea I, nr. 17
din 14 ianuarie 2003, cu modificările ulterioare.“
23. După articolul
25 se introduce articolul 26 cu următorul cuprins:
„Art. 26. – Anexele
nr. 1–3 fac parte integrantă din prezenta lege.“
24. Anexele nr. 1
şi 2 vor avea următorul cuprins:
„ANEXA
Nr. 1
L I S T A
cuprinzând categoriile de produse
cosmetice
– Creme, emulsii, loţiuni,
geluri şi uleiuri pentru piele (mâini, faţă, picioare etc.)
– Măşti pentru faţă (cu
excepţia produselor care acţionează ca abrazive superficiale ale pielii pe cale
chimică)
– Baze nuanţatoare
(lichide, paste, pudre etc.)
– Pudre de machiaj,
pudre după baie, pudre igienice etc.
– Săpunuri de toaletă,
săpunuri deodorante etc.
– Parfumuri, ape de
toaletă, ape de colonie etc.
– Preparate pentru baie
şi duş (săruri, spume, uleiuri, geluri etc.)
– Depilatoare
– Deodorante şi
antiperspirante
– Produse pentru îngrijirea
părului:
– nuanţatoare şi decolorante;
– produse pentru ondulare, îndreptare
şi fixare;
– produse pentru aranjare
(decorare);
– produse pentru curăţare (loţiuni,
pudre, şampoane etc.);
– produse de condiţionare (loţiuni,
creme, uleiuri etc.);
– produse de coafare (loţiuni,
lacuri, briantine etc.)
– Produse pentru ras
(creme, spume, loţiuni etc.)
– Produse pentru
machiaj şi îndepărtarea acestuia de pe faţă şi ochi
– Produse destinate
aplicării pe buze
– Produse pentru îngrijirea
dinţilor şi a gurii
– Produse pentru îngrijirea
unghiilor şi decorarea lor
– Produse pentru igiena
intimă externă
– Produse pentru băi de
soare (plajă)
– Produse pentru
bronzare fără soare
– Produse de albire a
pielii
– Produse antirid.
ANEXA Nr. 2 *)
Simbolul pentru indicarea perioadei
după deschidere
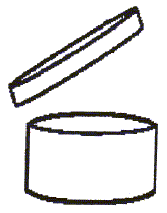
25. După anexa nr. 2
se introduce anexa nr. 3 cu următorul cuprins:
„ANEXA
Nr. 3 1)
Simbolul pentru precauţiunile
particulare de utilizare
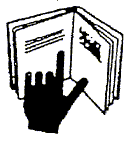
Art. II. – Limitele de competenţă în
efectuarea controlului pe piaţă al produselor cosmetice se stabilesc prin ordin
comun al ministrului sănătăţii şi al preşedintelui Autorităţii Naţionale pentru
Protecţia Consumatorilor, în termen de 180 de zile de la publicarea prezentei
legi.
Art. III. – Prezenta lege transpune
Directiva Consiliului nr. 76/768/CEE referitoare la produsele cosmetice,
publicată în Jurnalul Oficial al Comunităţilor Europene nr. L053 din 25
februarie 1977, cu modificările şi completările ulterioare, inclusiv cu cele
aduse prin Directiva nr. 2003/15/CE, publicată în Jurnalul Oficial al
Comunităţilor Europene nr. L066 din 11 martie 2003.
Art. IV. – Dispoziţiile prezentei legi
intră în vigoare la 3 zile de la data publicării în Monitorul Oficial al României,
Partea I, cu excepţia:
a) dispoziţiilor art. I
pct. 8 şi 9, care intră în vigoare la 180 de zile de la data publicării
legii;
b) dispoziţiilor art. I
pct. 6, 7 şi 10–19, care intră în vigoare la data aderării României la
Uniunea Europeană.
Art. V. – Legea nr. 178/2000 privind
produsele cosmetice, cu modificările şi completările ulterioare, precum şi cu
cele aduse prin prezenta lege, se va republica în Monitorul Oficial al României,
Partea I, dându-se textelor o nouă numerotare.
Această lege a fost
adoptată de Parlamentul României, cu respectarea prevederilor art. 75 şi
ale art. 76 alin. (2) din Constituţia României, republicată.
|
PREŞEDINTELE
CAMEREI DEPUTAŢILOR VALER DORNEANU |
PREŞEDINTELE
SENATULUI NICOLAE VĂCĂROIU |
Bucureşti, 28 septembrie 2004.
Nr. 379.